山澤凝暑氣,星漢湛光輝。在這個多彩的七月里����,由未來論壇機構(gòu)和畢馬威中國聯(lián)合舉辦的以“未來基因治療”為主題的前沿科學(xué)技術(shù)交流會如約而至。本次論壇匯聚了多位來自科研界�、臨床醫(yī)學(xué)界����、醫(yī)藥企業(yè)的大咖們,共同探討了基因治療的最新研究和臨床進展��。邦耀生物科學(xué)家�、華東師范大學(xué)吳宇軒研究員也受邀參加此次論壇,分享基因治療在β-地中海貧血上的最新研究進展�。
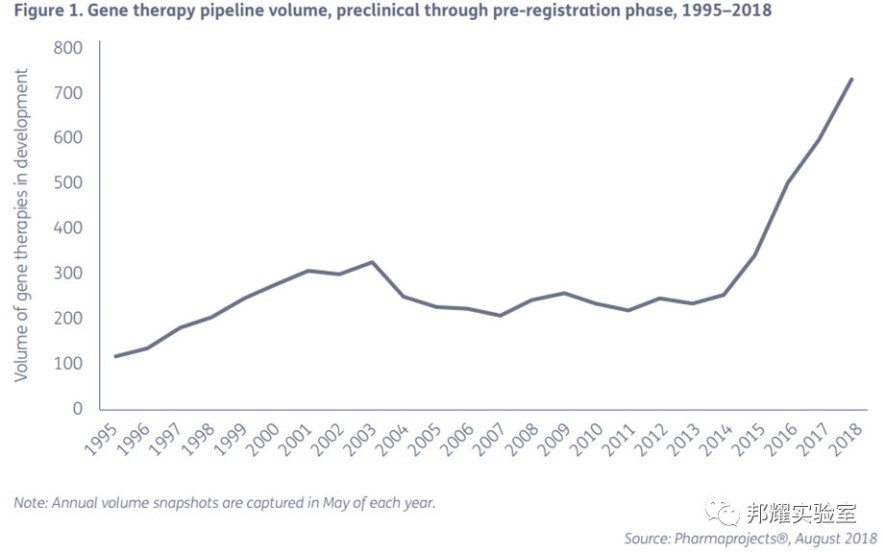
基因治療(Gene Therapy)是指將外源正常基因?qū)氚屑?xì)胞����,以糾正或補償缺陷和異常基因引起的疾病���,以達(dá)到治療目的�?�;蛑委熞云湟淮谓o藥終生治愈遺傳疾病的獨特潛力讓一切不可能變?yōu)橛锌赡堋O聢D展示了1995-2018年期間全球注冊并開發(fā)的基因治療與臨床項目的數(shù)量��,可以看到自2013年數(shù)量快速上升���,標(biāo)志著基因治療已經(jīng)進入高速發(fā)展階段�����。
1995年-2018年期間全球注冊并開發(fā)的基因治療與臨床項目的數(shù)量
β-地中海貧血(β-Thalassemia����,地貧)是一種由于β-珠蛋白(β-globin)亞基突變導(dǎo)致患者自身的成人血紅蛋白(HbA)異常的遺傳性疾病�,是全球分布最廣、累及人群最多的一種單基因遺傳病��。其中我國β地中海貧血的檢出率為0.67%(約935萬)���。地中海貧血的重癥患者大概有30萬��,我國的重癥地貧患者主要分布在廣東�����、廣西����、貴州、海南和云南等地����。異體造血干細(xì)胞移植是根治“地貧”的方法,但花費巨大��,且配型極其困難���,使得基因治療有望成為新的治療選擇。
邦耀科學(xué)家吳宇軒研究員發(fā)現(xiàn)���,利用基因編輯技術(shù)重新開啟胎兒期的γ珠蛋白的表達(dá)���,代替有缺陷的β珠蛋白,很有可能成為緩解甚至治愈地貧的方法�。
吳宇軒研究員作報告
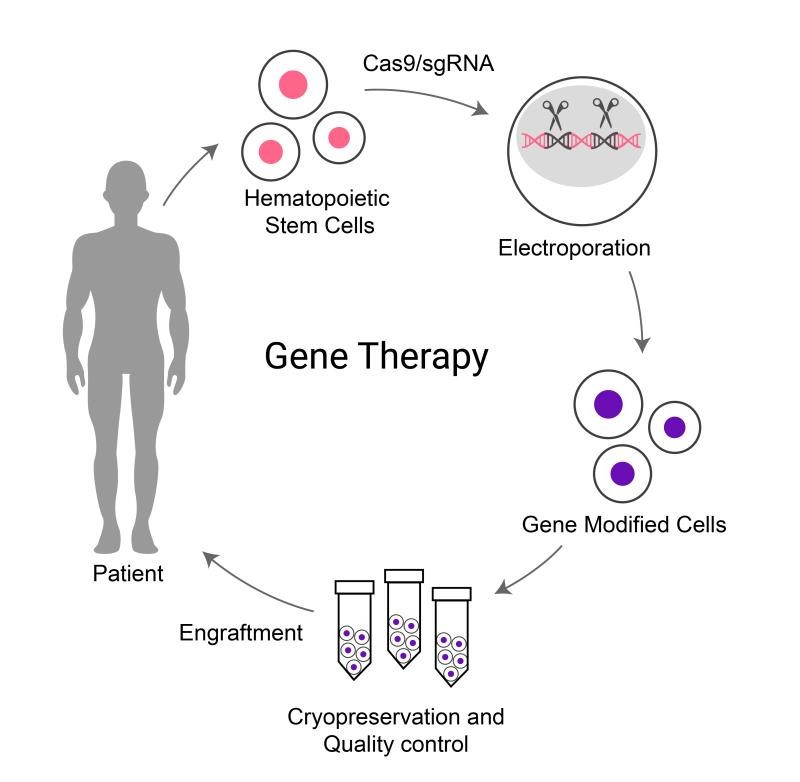
通過基因編輯技術(shù)編輯β-地中海貧血患者的造血干細(xì)胞中的BCL11A增強子位點,并進行自體造血干細(xì)胞移植����,所產(chǎn)生的HbF比例高達(dá)40%,因此足以起到治療效果���,從而有可能根治此類疾病��。最新的研究進展已于2019年3月發(fā)表在國際著名學(xué)術(shù)期刊《Nature Medicine》上�。
基因編輯治療地貧的策略
目前邦耀生物團隊正積極進行科技成果轉(zhuǎn)化,除了BCL11A位點�,還布局了自主知識產(chǎn)權(quán)的靶向HBG和HBB位點的臨床試驗,與國內(nèi)多家頂級醫(yī)療單位攜手�����,希望借此項研究及其臨床實驗的推廣���,使得基于基因編輯的基因治療成為我國β-地中海貧血患者全新的臨床治療方案����,不僅可以給廣大地貧患者帶來終身健康�,還可以極大減少我國血庫壓力。
與在基因治療方面處于領(lǐng)先地位的BlueBird Bio公司的慢病毒療法LentiGlobin (商品名:Zynteglo�,已獲得歐盟批準(zhǔn))相比,Zynteglo是一種基于慢病毒載體的體外基因療法���,且定價高達(dá)177萬美元����,名副其實的成為了全球第二昂貴的藥物!邦耀生物采用的將Cas9蛋白和sgRNA通過電轉(zhuǎn)染導(dǎo)入患者自體造血干細(xì)胞的治療方案���,更為高效�����、便捷和安全�,且成本極大降低�����。
在過去的一年里�,基因治療取得了一系列突破性的進展�����,大量研究成果進一步證明了基因治療在攻克多種人類嚴(yán)重疾病時的有效性和安全性���,我們相信基因治療這一創(chuàng)新療法將會為更多患者帶來福音���。